人工智能在电诊断学和神经肌肉医学中的作用:当前状态和未来方向
目前关于电生理与深度学习在医学诊断结合的研究还处在发展阶段,本次来学习一篇综述,概述了一下在神经肌肉病的诊断中可以使用的一些人工智能方案和技术。同时也指出目前仍存在的一些弊端,并为未来的研究方向提供了一些参考。
摘要
人工智能(AI)的快速发展,包括机器学习(ML)和深度学习(DL),在医疗保健领域带来了新的技术突破。这些技术正在改变我们利用医疗数据的方式,使疾病分类更加准确、诊断更加精确、治疗选择更加合理、治疗监测更加有效,并能进行高度准确的预后预测。不同的ML和DL模型已被用于区分正常个体与肌萎缩侧索硬化症和肌病患者的肌电图信号,准确率在67%至99.5%之间。DL模型在神经肌肉超声中也已成功应用,通过使用分割技术,对神经卡压疾病的诊断准确率至少达到90%,对炎性肌病的诊断准确率为87%。其他成功的人工智能应用包括预测治疗反应和预后,包括预测重症肌无力患者重症监护室的入院情况。尽管取得了这些显著进展,但在电诊断学和神经肌肉医学领域仍存在显著的知识、态度和实践差距。在这篇叙述性综述中,我们重点介绍了人工智能的基本原理,并将其与人类大脑网络的复杂性进行了对比。具体来说,我们探讨了人工智能在电诊断研究、神经肌肉超声以及神经肌肉医学其他方面的巨大潜力。尽管未来充满令人兴奋的可能性,但也有必要认识到并理解人工智能的局限性,并采取积极措施来应对这些挑战。通过战略性和负责任地整合人工智能技术,这一集体努力有望通过医疗保健的推进而取得巨大潜力。
关键词
人工智能、深度学习、电诊断学、肌电图、机器学习、神经肌肉医学、神经肌肉超声
1 引言
人工智能(AI)的概念自20世纪40年代开始发展,并包含各种定义。其中一个定义强调计算过程能够模拟通常与人类智能相关的功能,包括解释外部数据,并从这些数据中学习以实现特定目标。近年来,人工智能领域取得了指数级进步,这得益于“大数据”的可用性和计算能力的提升。人工智能已应用于我们生活的各个方面,如图像和语音识别、文本处理、自动驾驶以及医学领域。在医学领域,人工智能在放射学诊断、生理信号处理、遗传学以及个性化医疗方面取得了显著进展。医疗保健提供者现在期待人工智能在减少工作量、实时文档辅助、优化诊断、预测治疗反应以及改善患者预后方面带来益处。然而,也有人担心人工智能可能会威胁到工作安全,或产生不可预测、意外甚至有害的影响。
2 人工智能和深度学习的基
人工智能系统通过利用输入和结果数据来革新规则学习的方式。相比之下,传统的人类编写代码依赖于基于规则的系统(RBS),开发人员创建一套包含条件知识的情况-行动规则以产生期望的结果。然而,传统编程涉及繁琐的特定规则编码,严重依赖大量的先验知识,并且往往无法涵盖所有可能性。
相比之下,人工智能模型通过分析输入和输出数据的迭代过程来学习规则,使算法能够动态调整或修改数学方程,以准确表示潜在模式。这一过程基本上消除了耗时的手动规则编码需求。通过用足够大的数据训练模型,它能够熟练地在面对新输入时预测结果。
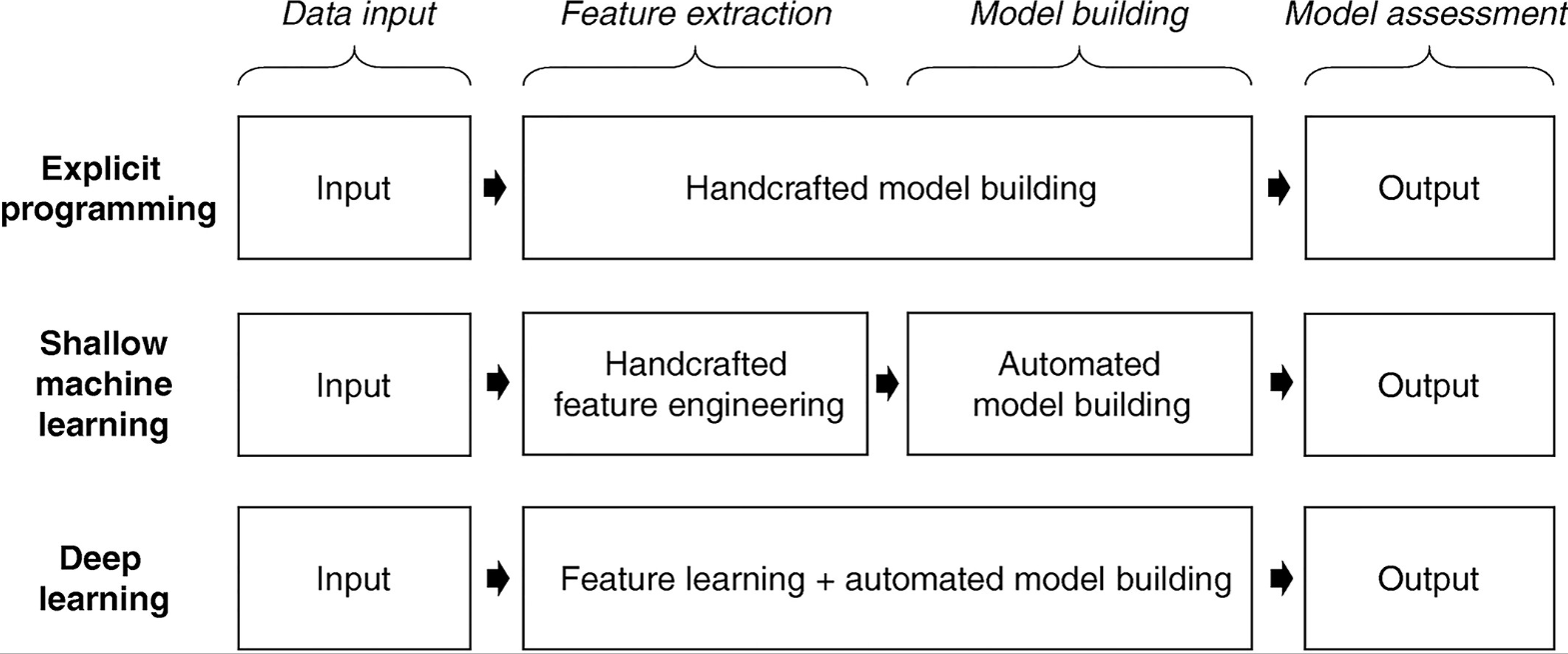
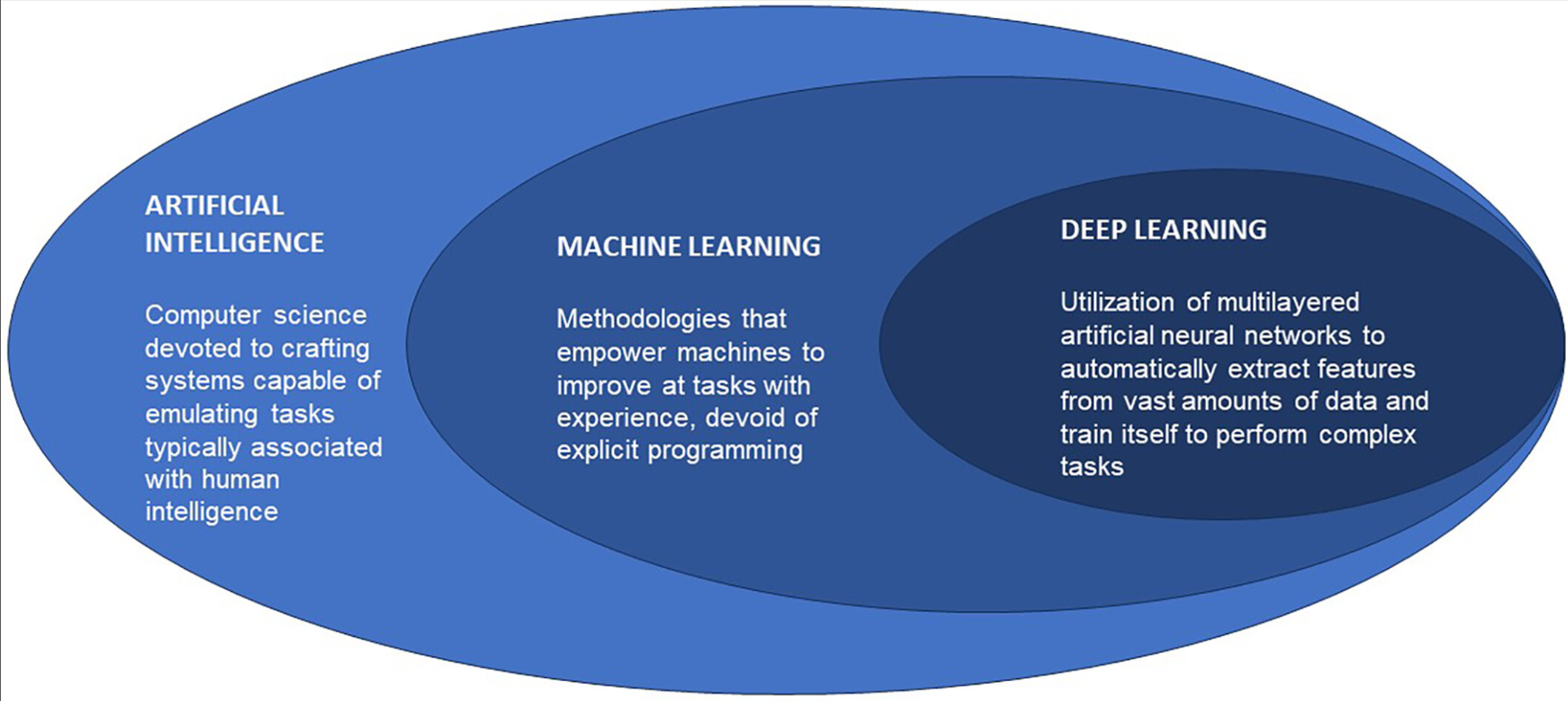
3 定义:人工智能、机器学习和深度学习
有关人工智能的术语虽相似但并不完全相同,如机器学习(ML)和深度学习(DL)。
机器学习是人工智能的一个分支,依赖于数据来使用算法学习如何执行任务。传统的机器学习算法,如线性回归、决策树和随机森林,旨在识别数据中的有意义模式或规则。
深度学习则是机器学习的一个分支,利用人工神经网络(ANN)。人工神经网络模仿人类大脑,由能够识别和表示知识及特定数据特征的计算算法层组成。例如,感知器和卷积神经网络(CNN)是深度学习的一种,常用于图像分类。通常,深度学习在处理大型和高维数据(如肌电图、图像)时更有用,而传统机器学习由于计算成本和速度要求较低,更适合用于低维数据环境。
在机器学习中,模型可以通过监督训练进行训练,即提供输入和输出(称为标签)以将输入映射到期望的输出。例如,一组标记为猫或狗的图像(输入)可用于训练模型。一旦训练完成,模型可以预测新图像是猫还是狗。
相比之下,无监督机器学习涉及没有特定标签的输入数据,模型在数据本身中学习模式和特征。例如,给定一组患者的健康记录,可以要求模型将具有相似健康状况的患者分组。
4 人工神经网络和深度学习的概念、功能和结构
受生物神经系统的启发,人工神经网络是由大量相互连接的小型处理器单元(即“神经元”)组成的巨大并行计算系统,每个单元执行特定的计算任务。
在生物系统中,神经元由树突接收来自相互连接神经元的脉冲信息,由胞体计算这些信息的总和,并通过轴突将输出传递给其他神经元。突触对收到的信息起调节作用,从而能够修改输入。人类大脑包含约1000亿个神经元,有60万亿个相互连接。
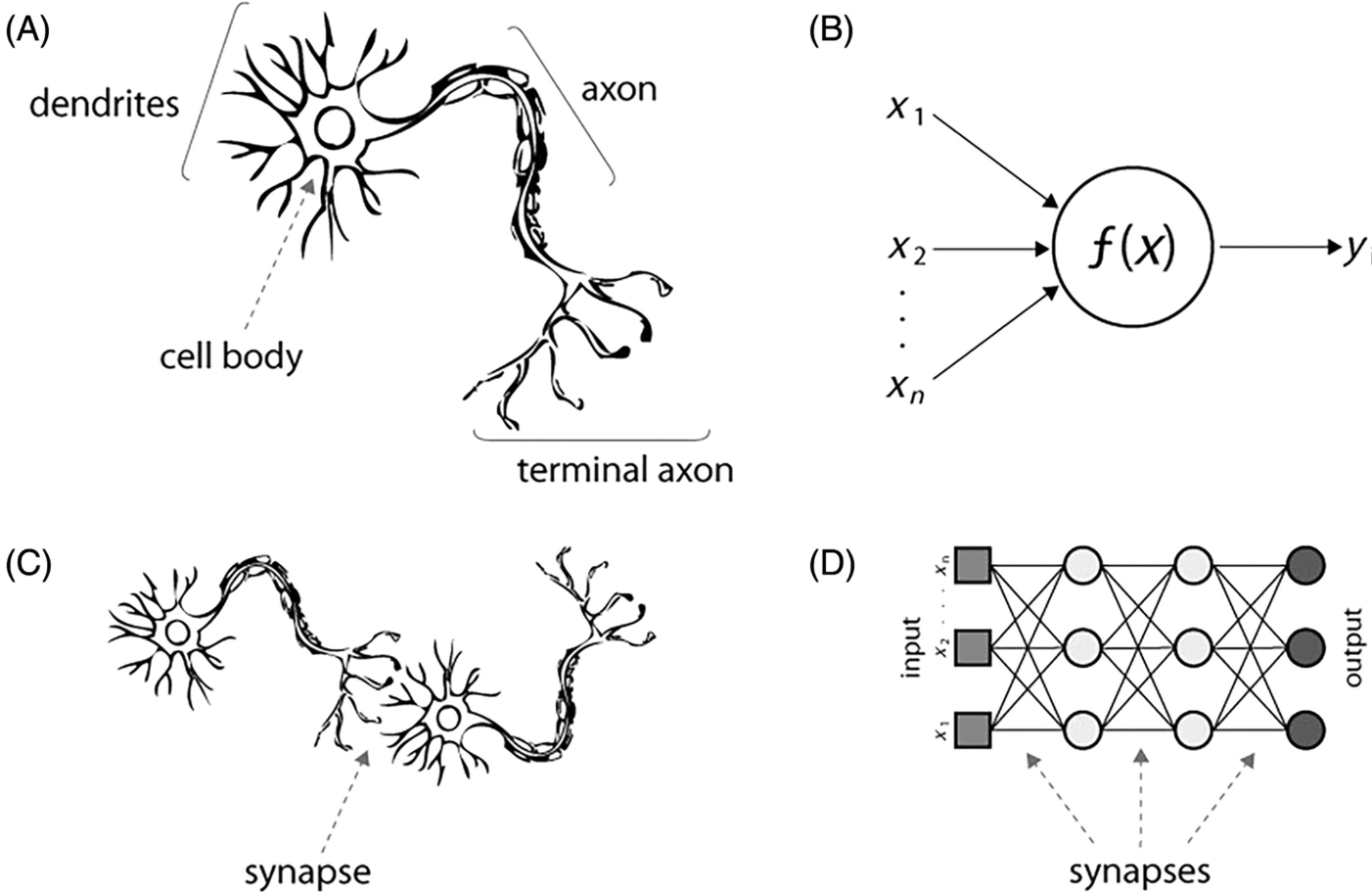
人工神经元单元的概念是由McCulloch和Pitts开发的。这个单元接收加权输入总和,应用激活函数,并在总和超过某个阈值时产生输出。Rosenblatt在20世纪60年代进一步开发了感知器,它是人工神经网络的基本单元。感知器是人工神经网络中受生物神经元启发的简化计算单元,能够进行二元分类。它通过应用加权总和和激活函数处理输入数据,产生二元输出。与传统的人类创建的基于规则的系统不同,神经网络通过使用代表性示例进行迭代训练,修改连接权重,从而学习输入和输出之间的特征和关系。这一特性使它们成为学习复杂模式的有吸引力的工具。
人工神经网络的功能包括:(1)模式分类——将表示输入(如文本、图像或信号)的特征向量分配到几个预定义类别之一。例如,将图像分类为猫或狗。(2)聚类或分类——这种无监督学习形式涉及算法在无标签数据组中寻找相似性模式。(3)预测或预测——预测时间序列中的未来样本。例如,根据随时间变化的先前房屋价值估算房屋价值,或根据先前行词预测句子中的下一个词,如在使用生成式预训练转换器(如GPT-4)等大型语言模型中所使用的那样。
感知器可以构建为多层,形成多层感知器。随着更多层的添加,神经网络的深度增加,形成了深度学习的概念。具有多层的深度神经网络(DNN)能够通过学习数据的层次表示来执行复杂任务。存在多种DNN架构,每种架构都有特定用途。表1列出了几种广泛使用的深度学习技术及其架构和功能。
5 人工智能在电诊断医学中的应用
5.1 针极肌电图信号的特性
肌电图波形数据是一种具有相对较高频率和振幅周期性变化的时序信号。该信号由每个时间步产生的电压值组成。当以50 kHz的采样率收集时,1秒的记录包含50,000个数据点,以微伏为单位进行测量。这些丰富的信息被认为是随机的、高维的,为运动单位的电特性提供了详细的见解。手动解释肌电图信号会导致显著的操作者间变异性,并且在归因分数或印象之前,实际上不允许评估所有肌电图数据点。肌电图数据的存储在记录设备之间有所不同,通常记录为每单位时间的电压值列。此外,还存储了诸如患者信息、研究检查细节(包括机构特定协议)以及所检查的具体肌肉等元数据。
5.2 肌电图信号预处理
在获取肌电图信号后,使用具有或不具有陷波滤波器的高低频截止滤波器对信号进行去噪。这些滤波器允许去除包括环境噪声在内的污染电压活动。
还开发了机器学习和其他数学模型,以减少或去除包括环境噪声在内的污染信号。另一种污染形式是在肌肉收缩和放松期间评估肌电图活动时的针极或患者运动伪影。这种类型的伪影更具可变性,难以使用简单的数学公式确定。因此,它构成了一个复杂的挑战,可以通过应用人工智能来解决。
在去噪和应用频率滤波器后,所得的肌电图信号可以被视为数据丰富的原始肌电图信号,准备进行人工智能处理。有多种可用技术可以从原始信号中提取有意义的特征,从而减少信号量、减轻输入拥塞,并优化人工智能模型的处理时间。
5.3 肌电图信号特征选择
肌电图信号分析的常规过程在某种程度上是主观的、劳动密集型的,并且可能受到操作者间变异性的阻碍,有时需要重复研究。此外,这种分析的准确性在很大程度上取决于执行人员的培训、技能和经验。然而,最近深度学习算法的进展在克服这些挑战方面非常有用。
原始肌电图数据本质上是复杂的,并且包含大量的信息,需要大量的计算资源和时间进行分析。主成分分析(PCA)提供了一种简化肌电图数据复杂性和多样性的方法,同时保留趋势和模式。PCA的主要目标是在不丢失重要信息的情况下降低这些数据的高“维度”。在使用肌电图数据的机器学习研究中,PCA的成功应用越来越多。
克服原始数据处理困难的其他策略包括开发新的特征提取方法,以从数据中获取特定的关键属性。这些提取技术通常分为时域(TD)、频域(FD)和时频域(TFD)。
下图显示了从正常参与者、肌萎缩侧索硬化症(ALS)和肌病患者中提取的肌电图信号特征的视觉样本。
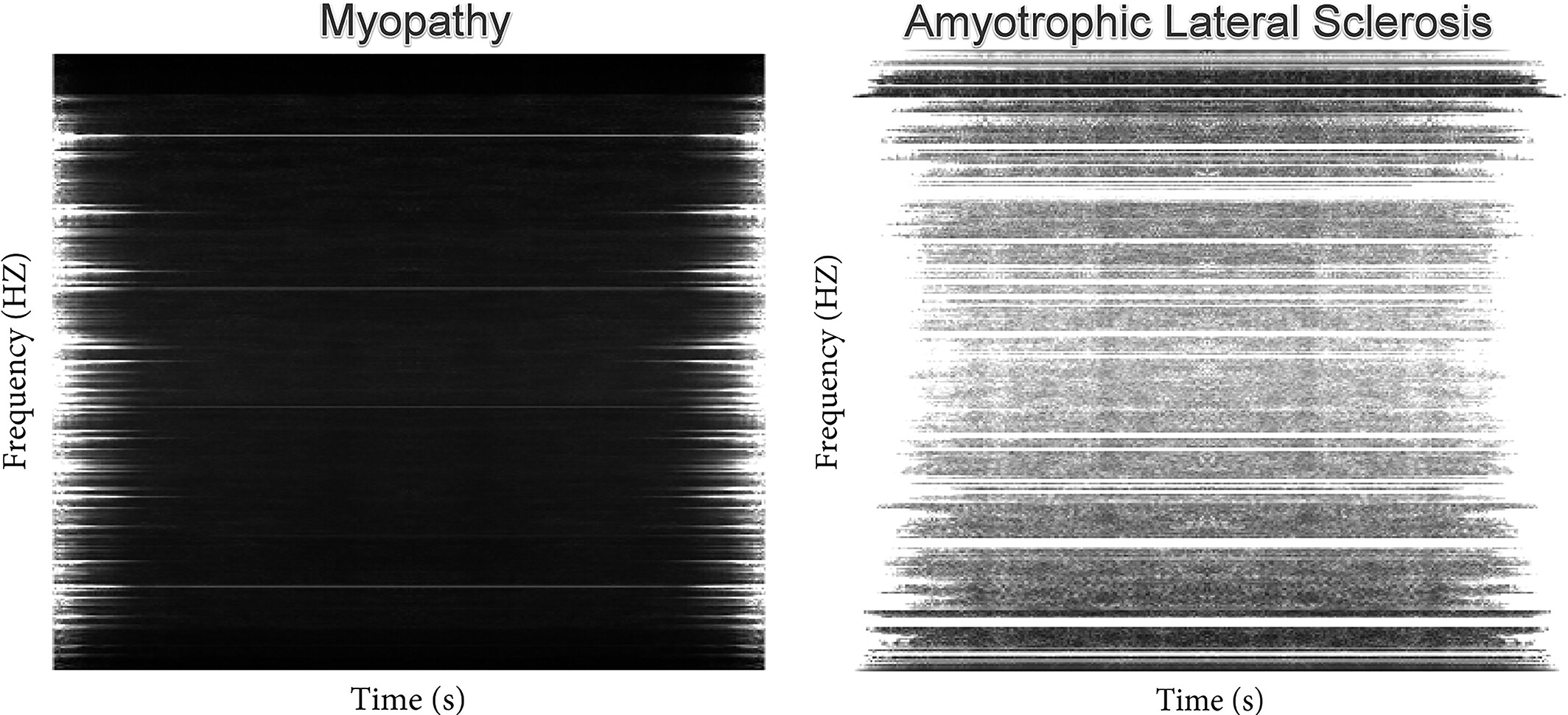
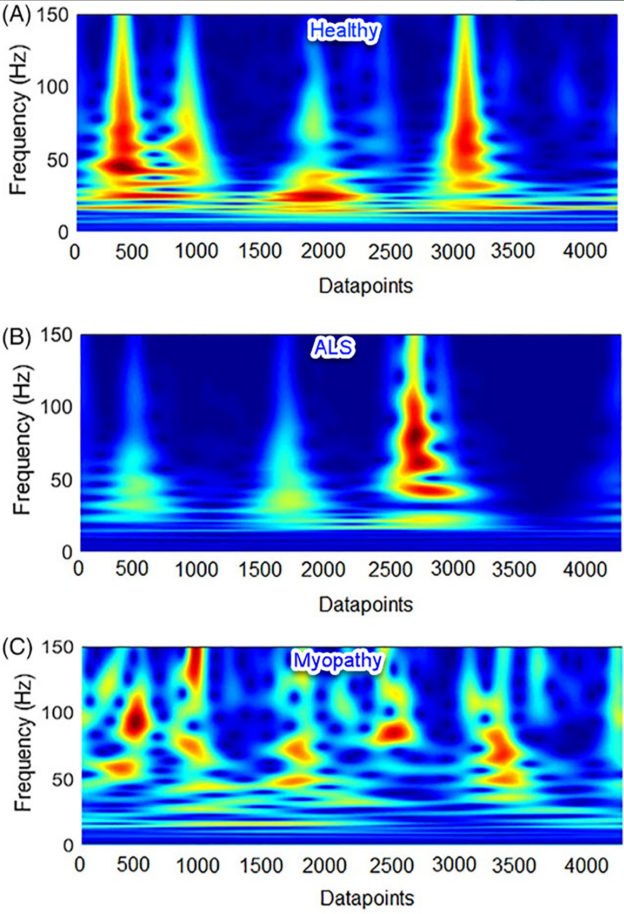
尽管这些技术的细节超出了这篇综述的范围,但每种技术都表现出独特的特征,并且传统上与具有相对有限计算能力的机器学习方法一起使用。
然而,深度学习的最新进展更好地促进了将原始数据作为肌电图分析的输入。深度学习模型能够有效处理原始肌电图数据中存在的大量信息,从而提高性能。接下来的部分将探讨这些进展,并突出深度学习模型的卓越能力。
5.4 肌电图信号数据库
目前,在电诊断医学领域,用于开发、测试和基准测试机器学习特别是深度学习算法的公开可用数据库非常有限。一个常用的数据库是由Nikolic在2001年作为博士论文的一部分发布的,其中包括来自相对较少个体的肌电图记录,其中包括7名被诊断为ALS的患者(3名男性,4名女性),年龄在52至67岁之间;10名健康个体(6名男性,4名女性),年龄在21至37岁之间;以及6名患有肌病的个体(4名男性,2名女性),年龄在19至63岁之间。尽管这个小数据集很受欢迎,但它并不能满足电诊断领域对代表性多样化和全面数据集的日益增长的需求。
5.5 肌电图信号分类
各种特征已被用作不同机器学习算法的输入,导致性能结果各异。在区分正常与肌病、正常与神经病或肌病与神经病时,分类性能有所不同。例如,使用K最近邻分类器的时域和频域技术在小数据集中区分ALS与正常时可以达到100%的准确率,但在区分肌病与正常时准确率仅为66%。众多的机器学习和深度学习技术也被使用,准确率各不相同。
额外的预处理步骤,如去噪技术,已被证明可以提高分类准确率。总体而言,分析单个运动单位动作电位(MUAP)的形态特征往往不如分析MUAP序列特征有效。同样,时域分析在与时间频率分析相比时表现不佳。这很有趣,因为人类专家在评估放电率和募集时主要依赖时域分析。
在探索深度学习结构时,发现不同的配置,如神经元数量和“隐藏”层数量,对性能有不同的影响,通常与预期结果偏离。在最近的一项研究中,使用随机森林分类器(RFC)的传统机器学习方法被用于将肌电图信号分为三类:正常、神经病和肌病。该研究涉及在自愿肌肉收缩期间从25名健康对照、20名ALS患者和20名包涵体肌炎(IBM)患者中收集肌电图信号。使用了5秒的片段,并自动提取了总共794个特征。结果表明,RFC算法在区分健康对照与ALS时准确率为0.78,在区分健康对照与IBM时准确率为0.68,在分类ALS与IBM时准确率为0.57。尽管这些发现表明传统机器学习算法可以用于肌电图信号分类,但深度学习算法在这一领域显示出更高的性能潜力。
最近的进展允许深度学习模型在无需手动特征提取的情况下对原始肌电图信号进行分类,从而实现更快、实时的应用,并且总体上需要的计算能力更少。一个显著的例子是ALSNet,它由三个卷积层组成,使用从10名健康个体和8名ALS患者收集的数据进行训练。值得注意的是,该模型在区分正常和ALS患者1秒片段的肌电图信号时达到了97.7%的准确率。然而,这些研究中使用的样本量有限,可能无法完全代表临床实践中遇到的神经肌肉疾病的多样性。因此,未来的工作必须解决这些不足。
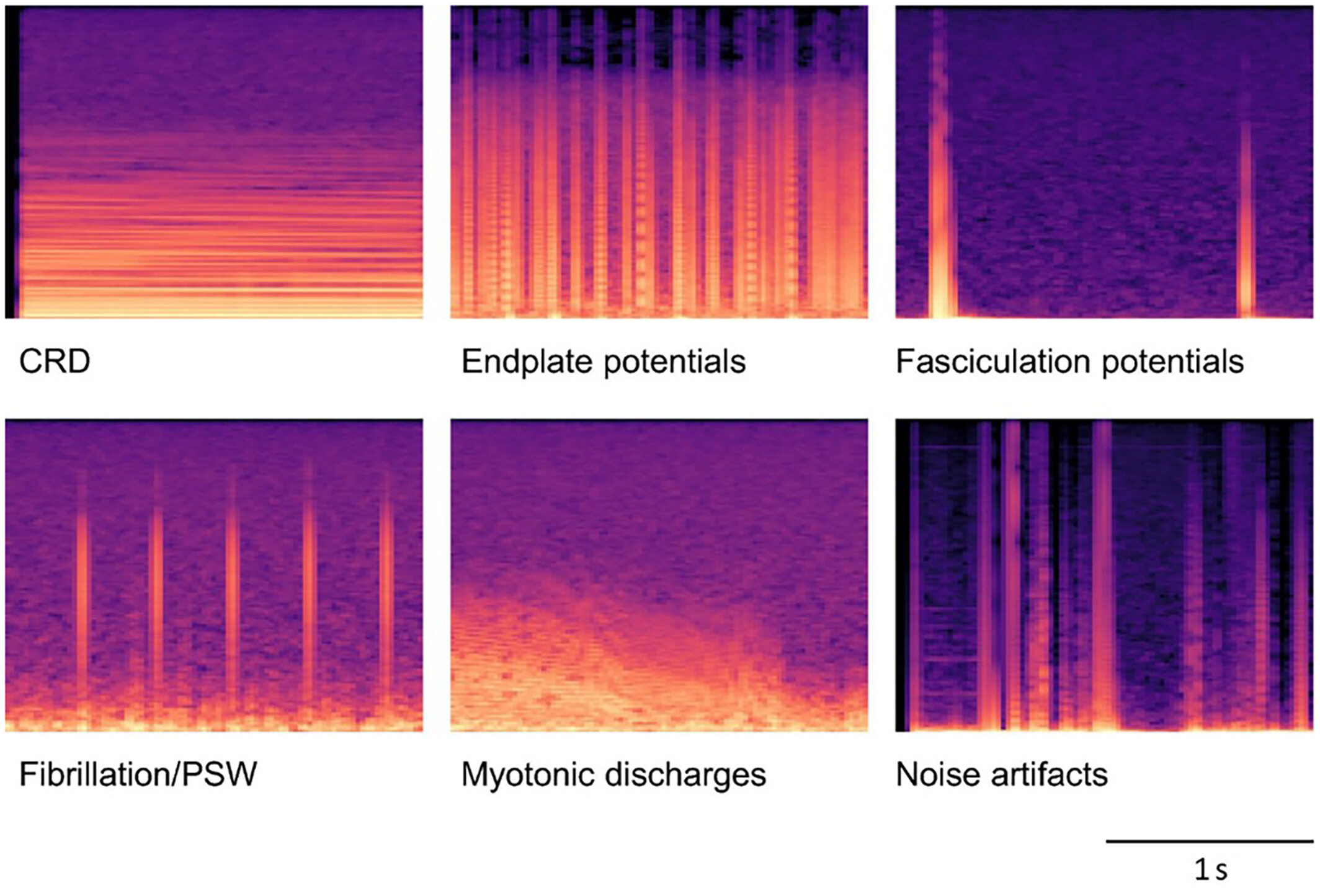
机器学习技术不仅在肌肉收缩期间的肌电图活动分类中证明了其有效性,还在自发活动(肌肉放松时的针极检查)的分类中得到了应用。在一项研究中,使用“梯度提升”等传统机器学习算法对六种不同的自发活动进行分类,包括复杂重复放电、肌强直放电、正锐波和/或纤颤电位、肌束颤动电位、终板电位和噪声伪影。该模型的总体准确率在89%到90%之间。另一项研究使用了深度学习模型,实现了更高的准确率,达到95%到97%。在这种方法中,肌电图信号被转换为梅尔频谱图图像,然后输入到卷积神经网络模型中。然而,值得注意的是,该模型存在一些误分类情况,例如将复杂重复放电误分类为肌强直放电,或将终板电位误分类为纤颤电位,这些也是人类专家常见的误分类。尽管如此,这些发现突显了机器学习尤其是深度学习技术在肌电图自发活动分类中的总体优势,以及在各种应用中提高诊断价值的潜力。
5.6 神经传导研究
神经传导研究(NCS)数据可以被分类为“结构化数据”,因为它们代表了包括振幅和速度等参数的离散值。这些值可以有效地组织成数值表格。这使它们与“非结构化”数据类型(如医疗笔记、肌电图信号和图像)区分开来。
一项显著的研究利用机器学习技术对糖尿病感觉运动性多发性神经病(DSPN)进行诊断和评估其严重程度。该研究使用了10个NCS变量,包括腓肠神经运动振幅和速度、腓肠神经感觉振幅和速度,以及中位神经运动和感觉研究的参数。利用集成机器学习算法,该研究在诊断和预测DSPN严重程度方面达到了93.4%的准确率。此外,机器学习方法突出了中位神经和腓肠神经传导研究具有最高的预测价值。
5.7 电气阻抗肌图
电气阻抗肌图(EIM)是一种相对较新的非侵入性测试,利用生物电阻抗技术评估神经肌肉疾病。EIM量化了肌肉在受到电流时的固有电阻和反应特性。鉴于神经肌肉疾病的诊断和监测存在诸多挑战,EIM通过提供评估肌肉健康状况的窗口,脱颖而出,可以评估肌肉的组成、大小以及萎缩或纤维化的程度。人工智能在EIM中的应用正在开辟新的可能性。研究表明,机器学习算法在分析复杂的EIM数据集方面具有实用性,包括在杜氏肌营养不良症、肌萎缩侧索硬化症和肥胖引起的肌肉萎缩的鼠模型中显著提高了分类准确率。EIM和人工智能之间的这种协同作用不仅提高了诊断准确性,还为改善神经肌肉疾病进展的监测提供了希望,这对于支持创新的治疗干预至关重要。
6 人工智能在神经肌肉超声中的应用
超声成像是一种快速发展的技术,在神经肌肉医学中发挥着重要作用。其应用范围从识别与机械损伤(包括神经卡压)相关的神经和肌肉病变,到与炎症和肿瘤相关的病变。
深度学习技术已经革新了超声成像中的图像获取,导致图像质量和处理速度的提升。机器学习在神经肌肉超声中的一个显著应用是腕管综合征(CTS)的检测和诊断。在这些研究中,神经肌肉超声图像被用作模型的输入,旨在将图像分类为正常或CTS。这些研究中报告的准确率很高,传统机器学习的准确率高达95%,深度学习的准确率高达98%。
此外,深度学习还被用于中位神经的精确分割,这涉及准确识别和定义神经结构的边界。这些分割技术显示出令人瞩目的准确率,从90%到95%不等。这一创新使得中位神经轮廓的自动和高效选择成为可能,从而有助于准确计算横截面积(CSA),这是神经肌肉超声诊断的关键参数。
最近深度学习的其他进展在无需提取CSA的情况下实现了CTS检测的卓越结果,一项研究的准确率达到了96%。可解释性测试显示,深度学习模型通过分析中位神经与周围软组织的回声性来做出准确诊断,从而为人类专家提供了潜在的学习特征见解。在术后腕管减压病例中,使用传统机器学习技术对CTS严重程度的预测通过曲线下面积分析达到了0.7-0.723的准确率。
此外,深度学习技术在自动识别其他神经卡压疾病方面也证明了有效性,例如肘部尺神经病变的准确率高达90%。
深度学习技术在神经肌肉超声肌肉成像中也显示出实用性。一个显著的应用是在具有挑战性的肌肉分割任务中,深度学习模型在识别肌肉轮廓和自动计算肌肉横截面积和回声性方面展示了接近人类水平的准确率。这可能有助于通过检测与去神经支配、肌炎或营养不良变化一致的改变,使用不同的神经肌肉超声特征来进一步表征肌肉疾病。深度学习基础的分割技术也已在其他肌肉骨骼组织(包括肌腱、骨骼、椎体和椎间盘)中进行了探索,显示出显著的准确率,有助于各种肌肉骨骼损伤的诊断和监测。
除了静态图像肌肉结构分析外,机器学习技术还被应用于神经肌肉超声视频帧,以检测肌束颤动。值得注意的是,机器学习在检测肌束颤动方面优于人类观察者,为研究以肌肉回声性和肌束颤动为特征的疾病(如运动神经元病)提供了新的机会。
深度学习方法还能够区分不同类型肌病(如皮肌炎、多发性肌炎和IBM)患者与正常个体的肌肉,准确率高达87%。
总体而言,包括深度学习在内的机器学习技术在推进神经肌肉超声领域方面显示出显著潜力,能够准确进行神经和肌肉分割,识别各种神经肌肉病理,并辅助诊断和监测越来越多的神经肌肉疾病。
7 人工智能在神经肌肉医学其他方面的应用
在医疗保健和神经病学领域,特别是在神经肌肉医学领域,人工智能的应用范围远超上述电诊断和神经肌肉超声领域。
人工智能在临床神经肌肉医学中的一个近期应用是其能够检测眼肌型重症肌无力(MG)患者在新斯的明给药前后眼部体征的变化,准确率达到了86%。人工智能模型基于U-net结构,这是一种用于目标分割的特殊神经网络,成功地分割并测量了眼睑和巩膜距离以及其他参数,使用患者图像作为输入。
在视频输入期间,面部运动也被人工智能模型用于诊断MG,MG诊断的准确率为87%,MG严重程度评估的准确率为94%。该模型在识别MG方面优于四位神经病学专家的平均表现,准确率达到了63%。此外,基于深度学习模型(DenseNet)在区分MG和非MG胸腺瘤患者方面显示出实用性,准确率达到了79%。
基于决策树的传统机器学习在基于结构化临床数据预测MG患者重症监护室入院方面也显示出价值,准确率达到了94%。该模型不仅预测ICU入院,还确定了最具影响力的临床预测因素,其中Myasthenia Gravis Foundation of America(MGFA)评分和胸腺瘤的存在是最重要的两个因素。此外,还开发了一种机器学习模型,基于21个临床因素预测MG患者的住院时间。这些例子突显了以结构化数据变量为输入的传统机器学习的有效使用。
尽管机器学习,特别是深度学习已被用于辅助ALS诊断,但其研究应用受到小样本量、模型性能差和泛化能力有限的限制。此外,这些研究通常仅将ALS患者与健康对照进行比较,而不是包括临床实践中常见的其他医疗(包括神经肌肉)疾病。然而,基于脑部磁共振成像(MRI)扫描获得的成像特征对ALS进行诊断的敏感性和特异性均达到了90%,显示了脑部MRI在自动化ALS检测中的潜在实用性。此外,模型在预测功能衰退和生存方面也显示出合理的性能。
深度学习在脑机接口(BCI)领域也发挥了宝贵的作用。用于运动命令的大脑信号可能因个体而异且存在噪声。尽管如此,基于深度学习的BCI模型已被开发用于ALS患者。这些模型通过头皮脑电图获取大脑信号,处理嘈杂的信号,并将其传输到外部设备,允许运动的准确率在88%到98%之间。
此外,机器学习,特别是深度学习还发现了其他多种临床应用,包括使用基因表达诊断散发性或家族性ALS患者,基于遗传数据预测ALS患者的认知障碍,使用表面肌电图信号诊断ALS,以及使用加速度计数据识别杜氏肌营养不良症患者的步态特征。深度学习模型还能够使用肌肉MRI数据区分面肩肱型肌肉营养不良症和肌炎,表现水平与放射科专家相当。
机器学习还通过提高参与者招募效率、实现模拟试验、辅助远程监测以及促进数字治疗(基于证据、临床评估的软件来管理或预防疾病)来提高临床试验效率。这些进步简化了试验流程,增强了数据分析,减轻了传统试验的限制,并引入了创新的治疗方式,可能改变了医疗干预方法。
8 医疗保健中人工智能的伦理和监管方面,包括神经肌肉和电诊断医学
随着人工智能技术的迅猛发展,监管机构在制定适当的指导原则方面难以跟上步伐。例如,美国食品药品监督管理局(FDA)对医疗设备和算法许可设定了严格的要求,通常在产品获批用于标准临床使用之前,需要大量的时间、精力和资金投入。为了应对技术的不断演变,FDA推出了一种新的监管策略,称为产品全生命周期,允许算法在开发和学习过程中进行持续修改,从而在整个生命周期内有效监管软件作为医疗设备。
尽管FDA的审批流程相对缓慢,但目前在评估和监管医疗领域,特别是神经病学领域所应用的算法方面,仍然缺乏一个稳健的框架。最近对53种应用于中枢神经系统的算法进行的系统回顾显示,只有10种算法经过同行评审发表,且缺乏严格的临床疗效研究,研究人群往往存在偏差。这些发现凸显了倡导并积极参与制定神经病学和神经肌肉医学领域人工智能应用监管框架的重要性。特别是在防止因过早部署医疗人工智能应用而可能产生的意外和非预期的伤害方面,这一点尤为重要,这些应用可能因开发不充分(包括模型训练不足)和上市前测试不完善。
9 医疗保健中人工智能的局限性,包括神经肌肉和电诊断医学
目前,医疗保健中的人工智能研究大多依赖回顾性数据来训练模型。这种方法限制了其在当代临床实践中的适用性,并阻碍了评估人工智能在前瞻性场景中的有效性。
此外,缺乏标准化的同行评审评估和稳健的方法学框架来评估和监管人工智能模型。与被认为是评估药物干预的黄金标准的临床随机、安慰剂对照试验不同,人工智能评估指标在许多情况下并不一致地与临床疗效或标准适用性对齐。
另一个重大挑战在于人工智能算法对新人群或更大临床环境的泛化能力。通常,这些算法在应用于不同机构或人群的数据时表现不佳。此外,一个令人担忧的局限性是算法偏差可能影响数据有限的患者人群,如少数种族群体,导致性能结果偏差。为了确保公平和公正,需要进行严格的主动努力,将训练数据分布在多个人群和环境中。
为了有效解决这些局限性,我们建议成立一个神经肌肉和电诊断医学特别工作组,致力于构建一个人工智能开发和应用的全面框架。这一举措应力求实现人工智能增强医疗保健提供者在该领域的影响,而不是威胁取代这些提供者。通过这样做,人工智能将因人类专业知识合作伙伴关系而更强大,这定义了增强智能。
增强智能是一种范式,侧重于人工智能在增强人类智能方面的支持作用,而不是取代它。该技术通过结合人类专业知识和算法准确性,丰富了临床决策,最终改善了诊断和治疗结果。例如,人工智能在肌电图中的应用有助于更细致地解释复杂的神经肌肉信号,从而辅助更精确地诊断各种神经肌肉疾病。人类临床医生不可替代的经验知识与人工智能提供的细致、数据驱动的见解相结合,最终推动了改善患者预后和个性化神经肌肉医学的未来。
10 结论和未来方向
总之,尽管未来充满令人兴奋的可能性,但有必要认识到并理解人工智能的局限性,并采取积极措施来缓解这些挑战。通过倡导共同努力和富有成效的合作,我们可以积极引导人工智能的发展,确保在领域中实现增强智能。在此过程中,我们也应致力于提高所有可能从中受益的患者群体的安全性、公平性和公正性。这一集体努力通过战略性和负责任地整合人工智能技术,具有通过医疗保健推进而取得巨大潜力。
迈尔诺医疗紧跟研究热点,推出以下适用于面部肌电研究的传感器产品:分布式肌电传感器、FPCB高密度阵列式肌电传感器、分散式肌电传感器;织物式肌电传感器,适用研究领域:神经性面瘫、表情分析、情感识别、人机交互、口语训练等,如您对面部表面肌电图(sEMG)感兴趣,欢迎随时与我们联系,我们乐意为您提供更多信息与技术支持。
迈尔诺医疗致力于成为全球领先的生物信号装置供应商。通过整合远程数据管理平台和可穿戴生物传感器设备,实现长期健康指标跟踪与监测,形成对生活方式、心理状态、体征参数等的完整解决方案。可为体能训练、医疗康养、慢病监测、教学科研等行业提供国内领先的硬件与数据服务。
相关产品与科研支持

关于迈尔诺医疗
